Tarmfloraen og innflammatoriske tarmsykdommer (IBD)
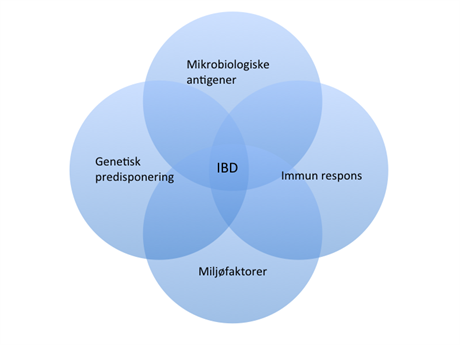 En kombinasjon av fire faktorer bidrar i IBD
En kombinasjon av fire faktorer bidrar i IBD
Innflammatoriske tarmsykdommer (IBD) består av ulcerøs kolitt og Crohn´s sykdom som begge er kroniske sykdommer med gjentagende episoder av inflammasjon i tarmen. Ulcerøs kolitt karakteriseres ved blødninger i overflatevevet i tarmen og er lokalisert til tykktarmen. Crohn´s sykdom oppstår både i tynntarmen og i tykktarmen og her kan betennelsen gå dypt ned i tarmvevet.
Den eksakte årsaken til disse sykdommene er ikke endelig definert. Vi vet at genetiske, miljømessige og bakteriologiske faktorer er invovert i sykdomsforløpet i tillegg til et immunsystem som ikke fungerer tilfredstillende.
Det er identfisert omkring 100 gener som predisponerer for IBD sykdom. Noen av genene er felles for både Crohn´s sykdom og ulcerøs kolitt og andre er knyttet til en sykdom alene.
Det er økende bevis for at IBD kan ha sin årsak i en unormal og øket immunrespons som følge av eksponering til sin egen mikroflora og at dette skjer hos genetisk predisponerte individer.
Den underliggende immunresponsen i IBD involverer endringer i balansen mellom proinnflammatoriske og immunregulerende cytokiner i tarmmukosaen. Pasienter med IBD har også en øket permeabilitet som gjør dem mer utsatt for direkte eksponering til tarmfloraen.
Det er vist at pasienter med IBD har en gastrointestinal ubalanse i tarmfloraen (dysbiose) i forhold til friske individer. Ubalansen er karakterisert ved et redusert mangfold av vanlige bakterier og tilstedeværelse av bakterier i tarmfloraen som en vanligvis ikke finner hos friske individer. Tarmfloraen hos IBD pasienter er også karakterisert av en lavere andel av bifidusbakterier i tarminnholdet og på overflaten i tarmmukosaen.
Et øket forbruk av antibiotika kan gjøre oss mer sårbare mot sykdom på lengre sikt. En alvorlig konsekvens av et øket forbruk av antibiotika er at antibiotika dreper våre godartede bakterier i samme slengen som de tar livet av de sykdomsfremkallende bakteriene. I noen tilfeller vil ikke den opprinnelige og godartede tarmfloraen i tarmen bli restituert etter en eller flere antibitikakurer. En slik langvarig endring i vår tarmflora kan øke vår sårbarhet overfor infeksjoner og kronisk sykdom.
En svekket tarmbarriere kan være en årsak til inflammatorisk tarmsykdom
En god tarmbarriere er svært viktig for å forhindre igangsetting og oppblussing av inflammatorisk tarmsykdom. Tarmbarrieren består av et cellelag av epitelceller (enterocytter og colonocytter) hvor det også sitter spesialiserte immunceller som skal beskytte tarmepitelet mot skadelige bakterier. I tarmepitelet sitter det også spesialiserte goblet celler som skiller ut mucus som skal danne et beskyttende slimlag over epitelcellene. I en normal tarm er den indre delen av dette slimlaget sterilt og fritt for bakterier mens det i det ytre slimlaget sitter bakterier. Bakteriene i det ytre slimlaget kommuniserer med det medfødte immunsystemet og informasjon sendes via det enteriske nervesystemet og vagus nerven til hjernen. Hjernen prosesserer informasjonen og sender informasjon tilbake til immunsystemet. Dette kalles tarm-hjerne aksen. Vi snakker og kommuniserer altså med våre egne bakterier.
Denne tarmbarrieren er i balanse og holdes vedlike ved hjelp av bakteriene eller mikrofloraen i tarmen. De godartede bakteriene produserer næringsstoffer som tarmepitelet er avhengig av. Disse næringsstoffene kalles kortkjedete fettsyrer og kommer fra fermenteringen av komplekse kostfiber eller prebiotika.
Tarmbarrieren kan bli skadet pga mavetarm infeksjoner, dårlig kosthold, stress, alkohol og andre miljøfaktorer. Da kommer det til bakterier som bryter i gjennom det sterile slimlaget og som setter i gang en immunreaksjon fra det medfødte og adaptive immunsystemet. Ved IBD sykdom vil en genetisk predisposisjon gjøre at det oppstår en betennelse i tarmvevet. Dette skjer antagelig fordi det medfødte immunsystemet ikke fungerer godt nok til å reparere skaden i tarmbarrieren.
Det er dermed et mål å forsøke å reparere denne viktige tarmbarrieren og sørge for at den blir tett slik at betennelse ikke oppstår.
Noen kostholdsfaktorer øker sjansen for å få tarmsykdom
Det er vist tidigere at svovelholdige forbindelser forårsaker kolitt i dyremodeller ved å øke permebiliteten og svekke tarmbarrieren i tykktarmen. Pasienter med UC har en signifikant høyere konsentrasjon av hydrogensulfid i avføringen og sykdomsaktiviteten korrelerer med konsentrasjonen av hydrogensulfid.
Det er gjort noen studier som har sett på sammenhengen mellom kostholdsfaktorer og øket sjanse for å få oppbluss av IBD sykdom. I en studie fra 2004 ble 191 pasienter med ulcerøs kolitt fulgt opp i løpet av ett år. Kostholdet ble nøye registrert og sykdomtilstanden rapportert hver uke (klinisk kolitt aktivitetsindex). Formålet med studien var å undersøke om kostholdsfaktorer som kostfiber, mat som inneholder mye svovel, melkeprodukter og alkohol påvirket graden av oppblussing av UC sykdommen.
Det ble funnet en korrelasjon mellom et høyt inntak av kjøtt og særlig rødt kjøtt/bearbeidet kjøtt og øket sjanse for oppblussing av UC. Likedan ble det funnet en koorelasjon mellom alkohol og oppblussing av UC. Kjøtt består av protein/aminosyrer som inneholder svovel og dette kan øke innholdet av hydrogensulfid i avføringen med en resulterende toiksisk effekt på overflatevevet (kolonocyttene) tarmen.
Effekten av kostfiber og andre kostholdsfaktorer ved IBD
Det har vært motstridende resultater fra studier som har undersøkt effekten av kostfiber ved IBD. Dette er ikke så overraskende, da kostfiber består av en rekke forskjellige stoffer. I tillegg vil også dosering og lengden på studien ha effekt på resultatet av studien. Det er derfor anbefalt å se på effekten av spesielle typer av kostfiber som prebiotika. En oversikt over studier med kostfiber har vist at prebiotika og inulin/oligofruktose virker positivt inn på sykdomsforløpet ved IBD.
En måte å øke beskyttelsen mot oppblussing av IBD sykdom kan være å øke inntaket av spesielle typer kostfiber som prebiotika som så vil øke veksten av godartede bakterier i tarmen. Det er vist at inntak av prebiotika og inulin øker mengden av bifidus bakterier og andre godartede bakterier som produserer de viktige kortkjedete fettsyrene lokalt i tykktarmen (acetat, propionat og butyrat). Det er de kortkjedete fettsyrene og særlig butyrat som er så viktig for tarmhelsen og som virker betennelsesdempende og som bygger opp tarmbarrieren.
Middelhavedietten er en sunn diett for tarmen
 Middelhavsdietten er gunstig for helsen
Middelhavsdietten er gunstig for helsen
Inflammatoriske tarmsykdommer og en rekke andre autoimmune sykdommer er vanlige i vestlige kulturer, men finnes sjelden i utviklingsland i den tredje verden. Det er økende bevis for at diett og livsførsel spiller en betydelig rolle for utvikling av tarmsykdommer. Den store økningen i hyppigheten av IBD de siste tiår tilsier at dette kommer av miljøfaktorer og i mindre grad kommer av genetiske årsaker.
Hvilken diett skal man velge. Her er det foreløpig ingen konkret veiledning å finne fra medisinsk hold. Rådet opp til nå har vært at du kan spise hva du vil så lenge du tåler det. Utviklingen går fort og de siste 10 årene har det jevnlig kommet ny informasjon om betydningen av tarmfloraen (bakteriene) og mikrobiomet (bakteriene + deres genmateriale) for en god tarmhelse og for helse ellers i kroppen. Det er tid for å bruke denne informasjonen og forsøke å finne en diett eller kosthold som tar vare på vår tarmflora slik at denne kan beskytte oss og forhindre oppblussing av betennelse.
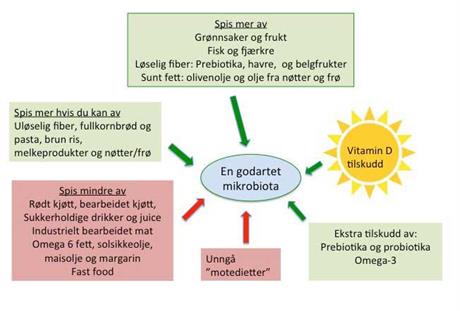
Det er mer typen av kosthold enn individuelle kosholdsfaktorer som er kritisk for en økning eller en reduksjon av risikoen for å få inflammatorisk tarmsykdom og annen kronisk sykdom med immunforstyrrelser. En middelhavsdiett karakterisert av et høyt inntak av frukt, grønnsaker, olivenolje, fisk, youghurt, grove kornsorter og nøtter kan være ønskelig for å forebygge inflammatorisk tarmsykdom og en rekke andre kroniske sykdommer. Et middelhavskosthold kan sammenlignes med det kostholdet som eksisterte på Kreta for 20-30 år tilbake. Det består av et kosthold som lager all mat fra bunnen av med et begrenset inntak av kjøtt og animalsk fett, ingen bearbeidete kjøttprodukter og et rikelig og stort mangfold av frukt og særlig grønnsaker.
Sukker, laktose, raffinerte meltyper og gluten unngås så langt det er mulig. Havre er gunstig for både tarmen og for å redusere kolesterolet.
Man skal være skeptisk til og helst unngå industrielle ferdigmat produkter som posesupper, sauser, dressinger etc, da disse inneholder tilsetningsstoffer og dårlige fettkilder (melkefett og omega-6 flerumettet vegetabilsk fett) som kan være skadelige for tarmen og redusere mangfoldet av bakterier i tarmen. Eksempler på skadelige tilsetningsstoffer er i særlig grad emulgeringsmidler og konserveringsmidler som kan skade tarmbarrieren. Lag all mat fra bunnen så vet du hva du putter i munnen.
For å forsterke den anti-inflammatoriske effekten i kostholdet så anbefales det å spise ekstra med både prebiotika og probiotika. Inntaket av vitamin D bør være tilstrekkelig og ligge over 50 mmol/liter eller helst over 75 mmol/liter. Alle bør sjekke dette hos sin fastlege.
Polyfenoler fra blåbær ser ut til å ha en god effekt på tarmfloraen. Dette er nok en god investering for å få en bedre tarmhelse.
Prebiotika styrker tarmbarrieren og stimulerer våre godartede bakterier
 BraMage Prebiotika-D3 inneholder 1g prebiotika og 5μg vit.D3
BraMage Prebiotika-D3 inneholder 1g prebiotika og 5μg vit.D3
Prebiotika stimulerer produksjonen eller formeringen av dine egne gode bakterier i tykktarmen. Eksempler på godartede bakterier er bifidus og laktobacillus bakterier. Denne forskyvningen mot godartede bakterier i tykktarmen er gunstig, da den hindrer skadelige bakterier å skape en ubalanse (dysbiose) i tarmfloraen.
Disse godartede bakteriene vil bidra til å øke produksjonen av særlig butyrat eller smørsyre (butansyre) i tykktarmen som har en godartet effekt på overflatevevet i tykktarmen. Smørsyre er den viktigste energikilden for overflatevevet i tykktarmen og er viktig for å holde dette friskt.
Prebiotika kan være med å skape en god tarmhelse på mange forskjellige måter:
- Rette opp en ubalanse i tarmfloraen slik at denne blir mer godartet og dermed fortrenge mer skadelige bakterier.
- Sørger for å støtte opp om vedlikehold og stimulering av tarmbarrieren og forhindre bakteriell translokasjon eller "lekk tarm". Dette reduserer mulighetene for at bakterier skal få direkte kontakt med immuncellene i tarmveggen og faren for at det skal oppstå en immunreaksjon i tarmvevet og betennelse i tarmen.
- Senker pH i tykktarmen noe som gjør det vanskeligere for skadelige bakterier å overleve.
- Stimulerer T-regulerende celler som reduserer betennelsesnivået
- Prebiotika sørger også for en regulering av tarmperistaltikken, noe som hjelper både de med for løs avføring og de som er obstiperte.
- Prebiotika øker absorpsjonen av kalsium, magnesium og jern fra maten og fra kosttilskudd.
Referanser
1. Influence of dietary factors on the clinical course of ulcerative colitis: a prospective cohort study, S L Jowett et al., Gut 2004; 53: 1479-1484
2. Review: Potential Benefits of Dietary Fibre Intervention in Inflammatory Bowel Disease, Celestine Wong et al., International Journal o Molecular Sciences, 2016, 17, 919
3. Review: An Examination of Diet for the Maintenance of Remission in Inflammatory Bowel Disease, Natasha Haskey et al., Nutrients 2017, 9, 259
4. Lifestyle-related disease in Crohn´s disease: Relapse prevention by a semi-vegetarian diet, Mitsuro Chiba et al., World Journal of Gastroenterology, 2010, May 28th, 16(20), 2484-2495.
